大好評!『HIFU(ハイフ)+Density(デンシティ)』の違いとは?
公開日:2024/07/29 更新日:2025/08/27![]()

今回ご紹介するのは
『HIFU(ハイフ)+DENSITY(デンシティ)』です🌟
以前ご紹介した頬のタルミや肌の張りにおすすめのデンシティですが、
ハイフと併用することの利点や、ハイフとの違いについてご説明していきたいと思います
✅ハイフとデンシティの違い
ハイフとデンシティは、どちらも手術や切開のように肌へ大きなダメージを与えずに、たるみやシワを改善していく
切らないたるみ治療・照射系のたるみ治療ですが、
その作用する層と特化する効果には大きな違いがあります。
🌈ハイフの特徴
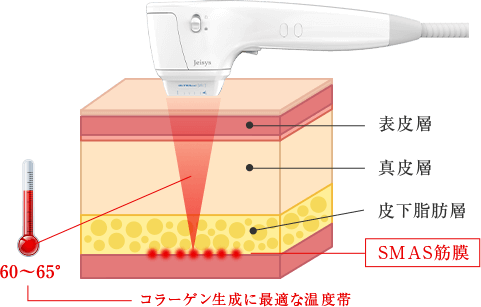
・高密度な超音波をSMAS層に集中させることにより、肌の土台である「SMAS(筋層)」のコラーゲンに直接作用し、「たるみ」を改善していきます。
・超音波を高密度に集束させてターゲットにピンポイント加熱することで、肌のハリをもたらすコラーゲンや線維芽細胞を作り出し、肌内部を活性化させます
・肌の土台となる筋膜からたるみを引き上げる
高密度焦点式超音波
◎皮膚は皮下組織を6.78MHzのRF(高周波)により加熱することで、真皮内のコラーゲン線維や皮下組織の線維隔壁を収縮することにより、肌のひきしめ(タイトニング効果)や小顔効果が期待できます。
◎熱による真皮の線維芽細胞への刺激は、コラーゲンやエラスチンの生成を促し、美肌効果をもたらします。
◎肌の内側から引き締める
まとめますと、
🔴ハイフはお肌を支えるSMAS層(筋膜)に熱を加え、深部の土台から引きあげる
🔵デンシティは表面から脂肪層に熱を加え皮膚表面からお肌全体をぎゅっと引締めるイメージです❕
実際に治療した方からお話を聞くと、
ハイフも『ジジジッッ』といった歯に響く感じの独特な痛みがありますが、
デンシティは『熱痛ッ?』といったハイフとはまた違う痛みがあるようです。
デンシティ+ウルトラセルZiの料金・費用
| ※部位は参考 | モノポーラ | モノバイ |
|---|---|---|
| ウルトラセルZi 650ショット + デンシティ100ショット |
55,000円 | 66,000円 |
| ウルトラセルZi 650ショット + デンシティ200ショット |
66,000円 | 77,000円 |
| ウルトラセルZi 650ショット + デンシティ300ショット |
77,000円 | 88,000円 |
頬のたるみが気になる、肌のハリが欲しいなどなど。。。
是非一度カウンセリングだけでもうけてみませんか❓❓
お気軽にご予約お電話お待ちしております✨
📞043-386-9138 肌と歯のクリニック東京ベイ幕張
また、当院のインスタグラムも実際に治療動画が載っていますのでよかったらご覧ください😊💕
📲Instagram ID:@hadatoha

施術名:ウルトラセルQ+
施術の内容
ULTRAcel Q+はHIFU(高密度焦点式超音波)というテクノロジーを使用し、皮下やSMAS筋膜に熱損傷を与えます。創傷治癒過程でコラーゲンが増成されることで、たるみを引き上げる効果が期待できます。治療のリスク・副作用
感染・熱傷・神経麻痺・色素沈着・毛包炎・紅斑
治療費
16,500円〜132,000円(税込)
治療期間
治療内容、個人差によって変わります。
通院回数
治療内容、個人差によって変わります。
医薬品・医療機器について
当製品は未承認医療機器です。Jeisys Medical Inc.より、医師が個人輸入しております。同一の成分や性能を有する他の国内承認医薬品等はありません。次の認証を取得しております。CE(2018.7)、MFDS(2018.5)
施術名:デンシティ
施術の内容
デンシティ(DENSITY)は、高出力な6.78MHzのRF(高周波)を使用してお肌のたるみやシワの改善が期待できるRF治療機器です。治療のリスク・副作用
感染、熱傷、色素沈着、毛包炎、紅斑
治療費
33,000円〜88,000円(税込)
治療期間
治療内容、個人差によって変わります。
通院回数
治療内容、個人差によって変わります。
医薬品・医療機器について
当製品は未承認医療機器です。
Jeisys Medical Inc.より、医師が個人輸入しております。
※承認を受けていない医薬品・医療機器については下記のページをご確認ください
https://www.yakubutsu.mhlw.go.jp/individualimport/health_damage/overseas_report/index.html
同一の成分や性能を有する他の国内承認医薬品等はありません。
MFDS(2023.04), FDA(2023.08),TFDA(2023.12)


